来源:格隆汇新股
近期,蓝纳成生物、百诺医药、珞石机器人、康华生物等一众山东企业迎来IPO新动态。
格隆汇获悉,烟台蓝纳成生物技术股份有限公司(简称:蓝纳成生物)于9月底递表港交所,以18A章规则寻求港股上市,由中金公司担任保荐人。
蓝纳成生物专注于肿瘤诊疗放射性药物的研发,也就是核药。核医学领域目前仍处于发展初期阶段,那么公司的研发管线进度如何,让我们一起通过招股书来一探究竟。
01
分拆自东诚药业,深创投押注,估值约33亿元
蓝纳成生物由东诚药业于2021年1月成立,总部位于山东省烟台市,2024年11月转制为股份公司。
截至2025年9月22日,东诚药业持有蓝纳成生物43.95%的股份,为控股股东。
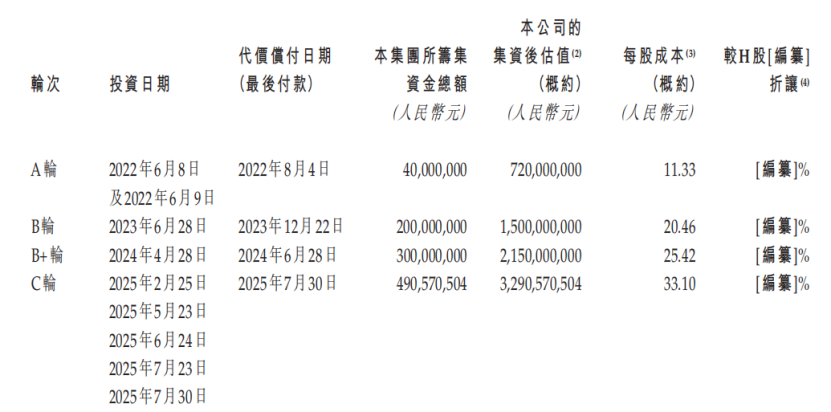
蓝纳成生物的主要机构投资者包括山东新动能、景林资本、深创投、前海方舟、烟台市国资委等;2025年7月,公司的投后估值约为32.9亿元。
融资情况,来源:招股书
公司董事会由九名董事组成,包括三名执行董事、三名非执行董事及三名独立非执行董事。
今年50岁的吴晓明任执行董事兼总经理,他先后获得安徽大学生物化学学士学位、北京大学工程项目管理硕士学位。
吴晓明此前曾在安徽省先锋制药有限公司、北京大学药物信息与工程研究中心、东诚药业等公司担任研发与管理职务。
公司另外两名执行董事分别是34岁的董事会秘书兼联席公司秘书李季先生,以及32岁的财务总监袁春云先生。
蓝纳成生物是一家处于临床阶段的生物科技公司,致力于肿瘤诊疗放射性药物的研发,是中国少数同时开发诊断及治疗放射性药物的公司之一。
放射性药物是指含有与药学分子结合的放射性同位素的药物。放射性药物利用放射性同位素独特的特性,在非侵入性诊断影像,或者作为治疗剂方面发挥关键作用。
诊断放射性药物。诊断放射性药物释放的辐射与生物组织相互作用,通过正电子发射断层扫描(PET)或γ相机等影像技术,可在分子层面检测病变组织的功能变化、异常基因表达及生化代谢变化。
治疗放射性药物。治疗放射性药物旨在用于靶向治疗而非成像。治疗放射性药物的药物分子选择性地聚集于目标组织或肿瘤,以放射性同位素释放的辐射诱导目标细胞的局部DNA损伤,同时尽量减少对周围健康组织的伤害。
根据公开统计数据,美国有400多家核药房,全球共有600多家。2024年,全球放射性药物市场估值为80亿美元。
中国的核药房产能仍相对有限,主要集中在两家企业:中国同辐集团公司、东诚药业,二者均营运着30多家核药房。
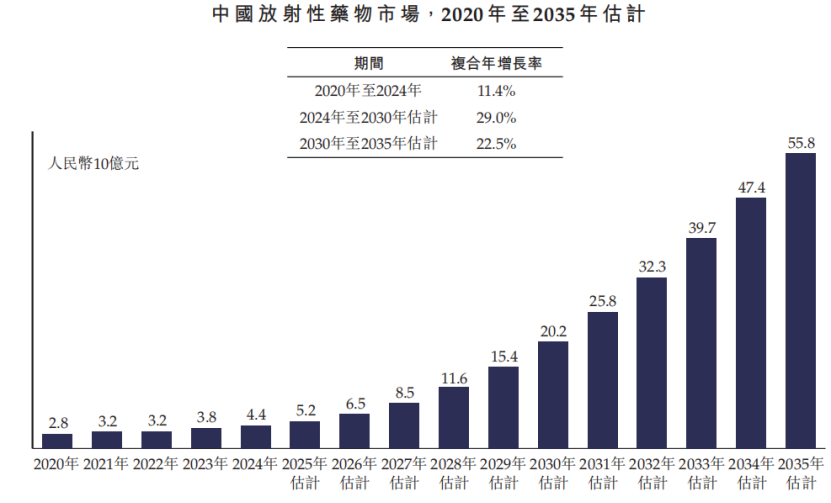
2024年,中国放射性药物市场估值为44亿人民币,仍处于低渗透状态,预计到2030年将增长至202亿元,同期复合年增长率为29%。
中国放射性药物市场,来源:招股书
02
18F-LNC1001是通过收购而来,处于III期临床阶段
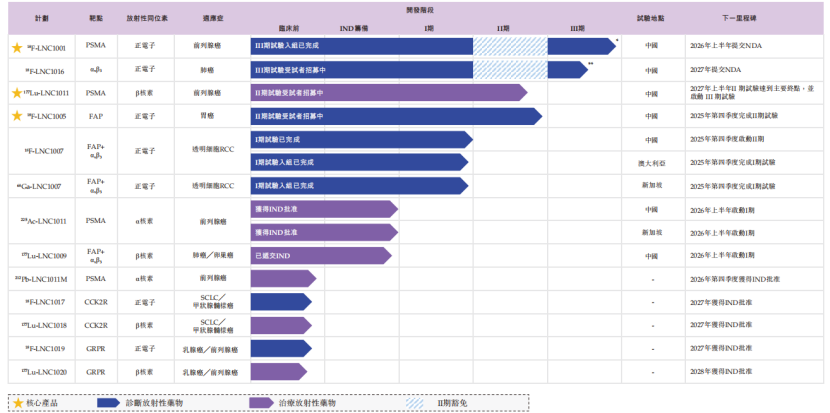
蓝纳成生物已建立由13款候选药物组成的管线,包括7款诊断放射性药物及6款治疗放射性药物。
其中,核心产品有3款,包括:
18F-LNC1001,是一款处于注册阶段的PSMA靶向候选诊断放射性药物,开发用于PSMA阳性前列腺癌患者的正电子放射断层扫描(PET)影像;
18F-LNC1005,是一款FAP靶向的候选诊断放射性药物,专为FAP阳性实体肿瘤(如胃癌)患者的PET影像而开发;
177LuLNC1011,是一款PSMA靶向治疗放射性药物,专门用于治疗PSMA阳性转移性去势抵抗性前列腺癌(mCRPC)。
公司主要在研创新药管线情况,来源:招股书
核心管线——18F-LNC1001
18F-LNC1001是中国首款进入III期临床试验的PSMA靶向放射性药物,其开发用于PSMA阳性前列腺癌患者的PET影像。
前列腺特异性膜抗原(PSMA)在90%以上的前列腺癌细胞上高度表达,该独特的表达谱使PSMA成为前列腺癌的标志分子,能够精准区分癌组织及健康组织。
公司预期将于2025年第四季度前完成18F-LNC1001的III期临床试验,并于2026年上半年向NMPA提交NDA。
截至9月22日,中国尚无获批具有放射性核素18F标记的PSMA靶向诊断药物。在中国,有4款PSMA靶向放射性诊断药物处于III期临床阶段,其中包括候选药物18F-LNC1001。
来源:招股书
值得注意的是,18F-LNC1001并非蓝纳成生物自研,而是通过收购而来。
LNC1001IP源自北京大学肿瘤医院,2020年5月,南京江原安迪科(东诚药业的全资附属公司)向北京大学肿瘤医院收购成功。
2022年4月,蓝纳成生物与南京江原安迪科订立技术转让协议,取得临床前阶段候选药LNC1001的全球独家权利及权益,并进一步将该药物开发为核心产品18F-LNC1001。
核心管线——18F-LNC1005
18F-LNC1005是FAP靶向候选诊断放射性药物,专为FAP阳性实体瘤(如胃癌)患者的PET影像而开发。
截至2025年9月22日,18F-LNC1005正处于中国II/III期联合试验的II期临床开发阶段,预期于2025年第四季度完成II期阶段,并于2026年上半年启动III期阶段,预期于2027年完成。
目前,中国及全球其他地区尚无用于诊断的FAP靶向放射性药物获批上市。中国有两款使用放射性核素18F标记的FAP靶向诊断放射性药物处于临床阶段,且都是蓝纳成生物的候选药物,分别是18F-LNC1005及18F-LNC1007。
核心管线——177Lu-LNC1011
177Lu-LNC1011是PSMA靶向治疗放射性药物,用于治疗PSMA阳性转移性去势抵抗性前列腺癌。
前列腺癌是男性泌尿生殖系统最常见的恶性肿瘤,主要影响65岁以上的男性。
全球前列腺癌药物市场预计将从2024年的193亿美元增长至2030年的324亿美元,复合年增长率为9.1%。
截至2025年9月22日,177Lu-LNC1011正处于II期临床开发阶段,预期于2027年上半年在中国177Lu-LNC1011用于PSMA阳性mCRPC成年患者的I/II期临床试验II期部分达到主要终点,并进入此项III期临床试验。
目前,共有3款前列腺癌治疗放射性药物获批,其中仅Novartis开发的Pluvicto在治疗阳性转移性CRPC及前列腺癌时靶向PSMA。截至同日,中国有8款PSMA靶向治疗放射性药物处于临床阶段。
03
尚未有产品销售,两年半亏损2.96亿元
目前,蓝纳成生物并无产品获批进行商业销售,亦无从产品销售中产生任何收益。
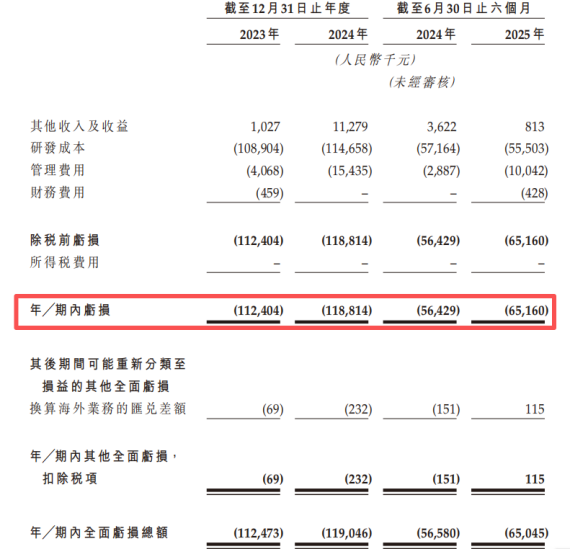
2023年、2024年、2025年1-6月(报告期),公司的收入分别为102.7万元、1127.9万元、81.3万元,主要来自利息收入、政府补助、投资收入等。
报告期内,公司的净利润分别为-1.12亿元、-1.19亿元、-6520万元,两年半累计亏损2.96亿元。
关键财务数据,来源:招股书
与其他研发阶段的创新药企一样,蓝纳成生物的亏损主要来自研发开支。
各报告期,蓝纳成生物的研发成本总额(含资本化进行中开发成本)分别为1.17亿元、2.35亿元、9010万元。
公司的研发团队由112名僱员组成,大多数曾在荣昌生物(09995.HK;688331.SH)、Quintiles(IQV)、恒瑞医药(01276.HK;600276.SH)、绿叶制药(02186.HK)及鲁南制药等知名企业从事研发工作。
截至2025年7月31日,蓝纳成生物的现金及现金等价物约3.68亿元,考虑到现金消耗率,公司的营运资金可以支付未来12个月至少125%的成本,包括研发成本、管理费用及其他经营成本。
值得注意的是,因放射性衰变,候选核素药物稳定性具有时限,因而保质期有限,通常为8至72小时。
尽管与传统药物的生产相比,其规模相对较小,但其所涉及的多个方面对小型制造商有相当高的要求。
因此,该等候选药物的生产设施需要靠近最终客户,其制造过程必须每周运转一次,且其需要有复杂的预先规划的物流来分发药物。
总体而言,蓝纳成生物所在的核医学领域目前仍处于发展初期阶段,未来渗透率有一定的提升空间,但是由于核药的生产和转运均需要严格的条件,所以药物获批后的放量速度大概率很难快速提高。
未来,蓝纳成生物能否顺利推进临床和商业化,格隆汇将保持关注。